การลงทะเบียนงานวิจัยทางคลินิกในฐานข้อมูล Thai Clinical Trials Registry (TCTR)
สืบเนื่องจากหลักเกณฑ์ทางจริยธรรมการวิจัยในคนในปฏิญญาเฮลซิงกิ ฉบับปรับปรุง ครั้งที่ 8 เมื่อปี ค.ศ. 2008 (พ.ศ. 2551) ข้อ 19 ระบุว่า “Every clinical trial must be registered in a publicly accessible database before recruitment of the first subject” และ International Committee of Medical Journal Editors (ICMJE) ได้บังคับใช้การลงทะเบียนนี้แล้วตั้งแต่ปี พ.ศ. 2548 และปัจจุบันนี้ได้มีวารสารต่างๆ จำนวนมากขึ้นเรื่อยๆ ที่แม้มิได้มีรายชื่ออยู่ในกลุ่ม ICMJE แต่ได้นำ Recommendation ของ ICMJE มาบังคับใช้ จึงเป็นเงื่อนไขว่า จะไม่รับตีพิมพ์ผลงานวิจัยทางคลินิกที่ไม่ได้ลงทะเบียนไว้ในฐานข้อมูลสาธารณะ ซึ่งผู้วิจัยจะต้องลงทะเบียนงานวิจัยก่อนทำการวิจัยในอาสาสมัครรายแรกเสมอจึงจะเป็นไปตามข้อบังคับของ ICMJE แต่ในขณะนี้ยังมีนักวิจัยส่วนหนึ่งที่ไม่ทราบข้อมูลดังกล่าว ทำให้พลาดโอกาสที่จะได้รับตีพิมพ์ผลงานวิจัยในวารสารทางวิชาการชั้นนำ
ดังนั้นการลงทะเบียนงานวิจัยแบบทดลองทางคลินิกจึงมีความสำคัญ ในการทำให้เกิดความโปร่งใสในการทำงานวิจัย เปิดโอกาสให้ผู้ป่วยได้มีส่วนร่วมในงานวิจัยเพิ่มขึ้น ลดความซํ้าซ้อนโดยไม่จำเป็นของงานวิจัย และยังเป็นแหล่งข้อมูลที่สำคัญสำหรับผู้กำหนดนโยบาย นักวิจัย และ ผู้ป่วย
คณะกรรมการจริยธรรมการวิจัยในคน กรุงเทพมหานคร จึงขอความร่วมมือให้นักวิจัยลงทะเบียนในระบบงานวิจัยแบบทดลองทางคลินิกของประเทศไทย (Thai Clinical Trials Registry: TCTR) ซึ่งเป็นแหล่งทะเบียนเดียวในประเทศไทยที่ได้รับการรับรองเป็น Primary Registry จากองค์การอนามัยโลก หรือระบบลงทะเบียนที่เป็นมาตรฐานสากล ได้แก่ ระบบลงทะเบียนขององค์การอนามัยโลก (International Clinical Trials Registry Platform ICTRP) หรือระบบลงทะเบียนของสถาบันสุขภาพในประเทศสหรัฐอเมริกา (ClinicalTrials.gov) เป็นต้น
-
แนวทางปฏิบัติในการนำข้อมูลย้อนหลังจากเวชระเบียนมาใช้ เพื่อการวิจัย3 มี.ค. 2567
-
แนวทางการทบทวนโครงการวิจัย : กรณีศึกษา - การประเมินคุณประโยชน์ต่อความเสี่ยงและกระบวนการขอความยินยอม9 ส.ค. 2567
-
การประเมินจริยธรรมการวิจัยในมนุษย์สาหรับโครงการวิจัยทางสังคมศาสตร์และพฤติกรรมศาสตร์9 ส.ค. 2567
-
Recruitment Process and Informed Consent9 ส.ค. 2567
-
การศึกษาวิจัยผลิตภัณฑ์สมุนไพรทางคลินิก27 กค. 2566
-
หลักเกณฑ์การพิจารณาเครื่องมือแพทย์23 กพ. 2566
-
การเสนอโครงร่างการวิจัย25 มีค. 2565
-
การรายงานเหตุการณ์ไม่พึงประสงค์ชนิดร้ายแรง (SAE)23 ธ.ค. 2564
The Forum for Ethical Review Committees in the Asian and Pacific Region (FERCAP)
FERCAP ก่อตั้งขึ้นในปี ค.ศ. 2000 ภายใต้โครงการ Strategic Initiative for Developing Capacity in Ethical Review (SIDCER) ขององค์การอนามัยโลก (WHO-TDR) เพื่อสนับสนุนการพัฒนาความสามารถในการพิจารณาจริยธรรมการวิจัยในภูมิภาคต่าง ๆ ทั่วโลก และแก้ไขปัญหาการวิจัยด้านสุขภาพที่สำคัญในภูมิภาค FERCAP เป็นหนึ่งในเครือข่ายระดับภูมิภาคทำงานร่วมกับองค์การอนามัยโลก UNESCO และองค์กรระหว่างประเทศอื่น ๆ ที่เกี่ยวข้องกับจริยธรรม
FERCAP เป็นองค์กรสำคัญในภูมิภาคเอเชียและแปซิฟิก ที่มีบทบาทในการประเมินและรับรองคณะกรรมการจริยธรรมการวิจัย การจัดประชุมเชิงปฏิบัติการ และการสนับสนุนโครงการที่เกี่ยวข้องกับจริยธรรมและการพัฒนามาตรฐานการวิจัย
SIDCER และ FERCAP ร่วมกันจัดตั้งมูลนิธิ SIDCER-FERCAP และได้พัฒนาระบบการรับรองคุณภาพจริยธรรมการวิจัยในมนุษย์ระดับชาติ และจัดการประชุมวิชาการเป็นประจำทุกปี โดยมีวัตถุประสงค์เพื่อให้ผู้เข้าร่วมประชุมได้รับความรู้และแนวทางปฏิบัติที่เหมาะสม ในการดำเนินการวิจัยที่มีจริยธรรมและคุณภาพสูง ในการประชุมมีการมอบรางวัล “FERCAP Accreditation Awards” เพื่อยกย่องความสำเร็จและส่งเสริมมาตรฐานในด้านจริยธรรมการวิจัย ให้แก่คณะกรรมการจริยธรรมการวิจัย (Research Ethics Committees - RECs) ที่ผ่านการประเมินตามเกณฑ์มาตรฐานของ SIDCER ซึ่งครอบคลุมประเด็นต่าง ๆ เช่น ความโปร่งใส ประสิทธิภาพ และการปฏิบัติตามมาตรฐานจริยธรรมสากล
The 24th FERCAP International Conference
Theme: Maximizing Benefits through Responsible of Research
ณ มหานครกาฐมาณฑุ ประเทศเนปาล ระหว่างวันที่ 24-27 พฤศจิกายน ค.ศ. 2024
มีผู้เข้าร่วมจำนวน 879 คน(onsite 550 online 329) จาก 25 ประเทศ

บุคลากรของกรุงเทพมหานครผู้เข้าร่วมประชุม ได้จัดทำอินโฟกราฟิกสิ่งที่ได้รับจากการประชุมที่สำคัญ เพื่อนำมาปรับใช้กับหน่วยงาน จำนวน 5 เรื่อง ได้แก่
-
สร้างสมดุลในงานวิจัย_ความเร่งด่วนและจริยธรรมในยุคโรคระบาดดร.พญ.เลิศลักษณ์ ลีลาเรืองแสง
-
Ethical Considerations in Climate Change and Neglected Tropical Disease Researchพญ.ชุลีกร โสอุดร
-
จะปกป้องอาสาสมัครเด็กอย่างไร ? การทำวิจัยในเด็กนพ.ไกรฤกษ์ สินธวานุรักษ์
-
การทดลองทางคลินิกแบบกระจายผศ.พญ.จิรัฐคณา จันทร์งาม
-
การพัฒนาระบบการเสนอโครงการวิจัยผ่านทางอิเล็กทรอนิกส์ศาสตราจารย์พิเศษมานิต ศรีประโมทย์
-
การรายงานการเบี่ยงเบนจากโครงร่างการวิจัย20 ม.ย. 2567
-
รายงานความก้าวหน้าของการวิจัย และขอต่ออายุการรับรองโครงร่างการวิจัย20 ม.ย. 2567
-
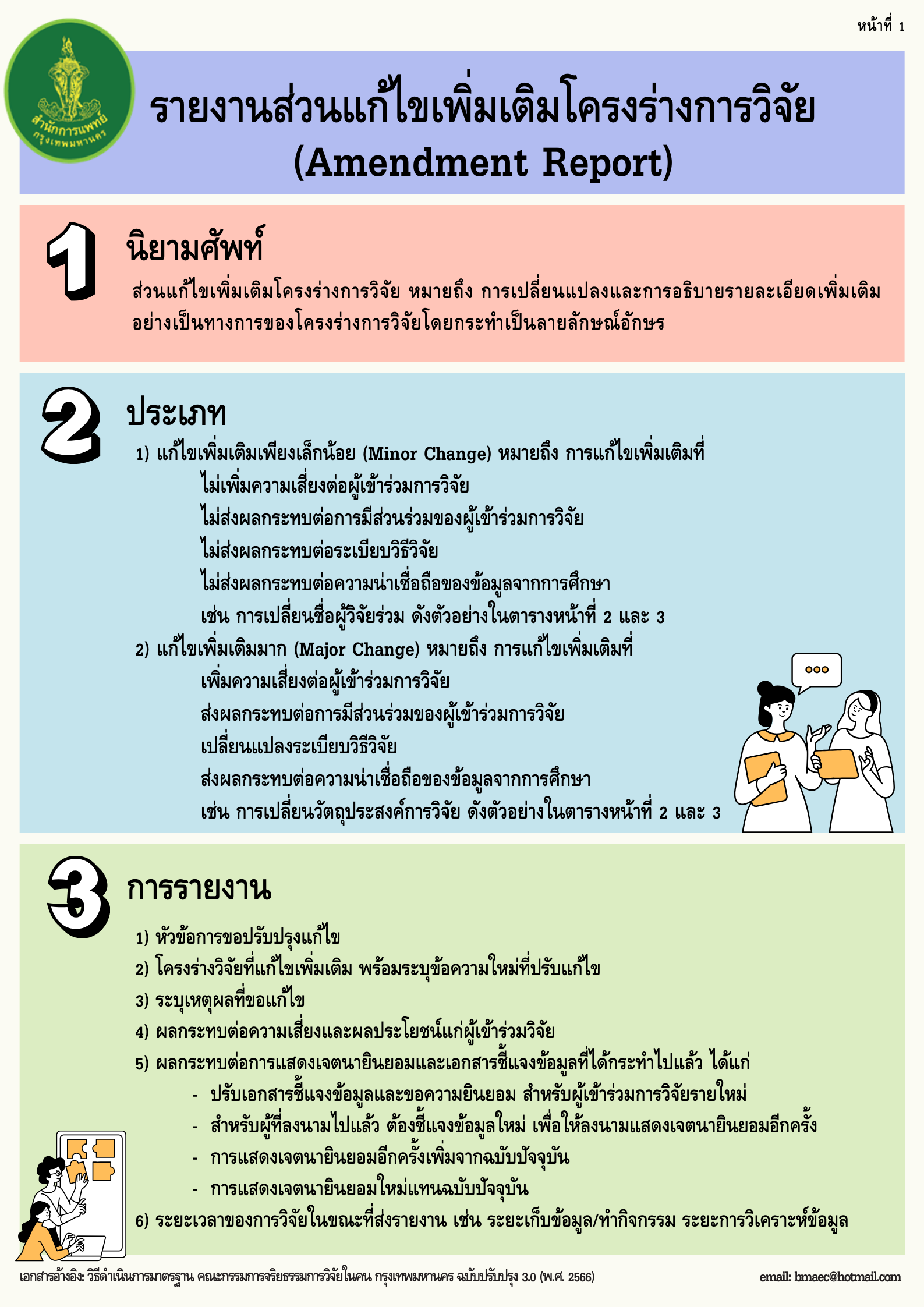
รายงานส่วนแก้ไขเพิ่มเติมโครงการวิจัย20 ม.ย. 2567
-
การขอความยินยอมเข้าร่วมการวิจัยในเด็ก15 ก.พ. 2567
-
การวิจัยในบุคคลกลุ่มเปราะบาง15 ก.พ. 2567
-
รายงานเหตุการณ์ไม่พึงประสงค์ชนิดร้ายแรง SAE15 ก.พ. 2567